Notre expertise spécifique sur les maladies à prion, la maladie d'Alzheimer (MA) et les cellules souches est à la base de nos recherches sur les mécanismes physiopathologiques et les approches thérapeutiques des maladies neurodégénératives.
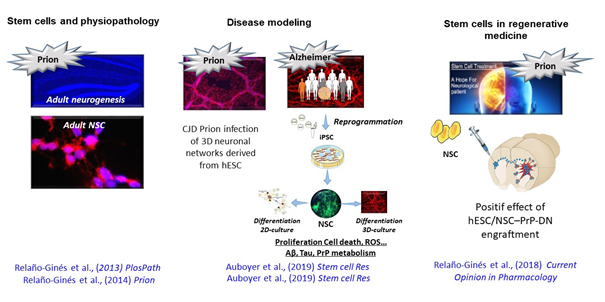
* Dans le but de développer une approche de médecine régénérative, nous avons utilisé des cellules souches neurales (NSC) dérivées à partir de cellules souches embryonnaires (ES) qui expriment des protéines prion (PrP) portant des mutations dites dominantes négatives (PrP) (PrP-DN) permettant d’inhiber la réplication du prion. Lors d’études précliniques utilisant des souris infectées par une souche de prion murine, nous avons montré une diminution de la vacuolisation, de l'astrogliose et de l'accumulation du prion. Notre objectif futur est de transférer cette approche thérapeutique sur des modèles humains dans la perspective d'aller vers des essais cliniques.
* Nous étudions également le rôle de la neurogenèse adulte et des cellules souches neurales (NSC) dans la propagation des prions. Nous avons montré que les NSC endogènes étaient non seulement infectées par le prion mais que leur potentiel de différenciation neuronale était également altéré. Nous avons également observé une augmentation de la prolifération et de l'apoptose dans les NSC infectées avec des prions par comparaison aux cellules contrôles non infectées. Notre objectif vise maintenant à déchiffrer les mécanismes moléculaires sous-jacents à ces phénotypes.
* Il n’existe actuellement que peu de modèles cellulaires pertinent pour étudier la maladie d’Alzheimer (MA). Nous avons récemment généré des cellules souches pluripotentes induites (iPSC) en reprogrammant des fibroblastes de patients atteints de MA génétique liée à une mutation dans les gènes APP et PS1 (iPSC-MA). Les cultures de réseaux neuronaux obtenus à partir des iPSC-MA ont montré une hyperphosphorylation de Tau et la présence d’agrégats Aβ. Nous avons également observé des altérations cellulaires dès le stade cellule souche (absorption du glucose, survie cellulaire, prolifération, différenciation neurale, diminution de la biomasse mitochondriale…). Par ailleurs, des observations basées sur l'ontogenèse du cerveau ainsi que sur des données cliniques conduisent à une nouvelle hypothèse étiologique selon laquelle certaines lésions de la MA apparaissant au cours du vieillissement pourraient provenir de dérégulations fines au cours du développement précoce du cerveau. Afin de « challenger » cette hypothèse, nous étudions des réseaux de neurones 3D et organoides de type mini-cerveaux imitant la corticogenèse à partir des iPSC-MA développées au laboratoire.